
 探索发现 · 交大智慧
探索发现 · 交大智慧
上海交大盛斌教授团队发表眼脑轴基座模型医工交叉成果
脑卒中作为全球致死和致残的主要病因之一,其防控始终是全球公共卫生的重大挑战。尤其是无症状性脑梗死(Silent Brain Infarction, SBI),作为脑卒中的“隐匿前驱病变”,在一般人群中患病率高达20%,却因缺乏典型临床症状而极易漏诊,显著增加后续卒中、痴呆及死亡风险。当前,SBI与脑卒中的临床检测高度依赖磁共振成像,其高成本与有限可及性严重制约了大规模人群筛查,亟须突破技术瓶颈以实现大规模人群筛查和早期干预。
在此背景下,上海交通大学计算机学院人工智能教育部重点实验室盛斌教授团队通过与清华大学医学院黄天荫教授团队及上海交通大学主动健康战略与发展研究院/医学院附属第六人民医院贾伟平教授和李华婷教授团队医工交叉合作, 并携手清华大学戴琼海教授团队及北京天坛医院王拥军教授等多学科团队联合攻关,近日在权威期刊Nature Biomedical Engineering发表题为“A deep learning system for detecting silent brain infarction and predicting stroke risk”的科研成果,创建全球首个眼-脑轴垂域基座模型—DeepRETStroke系统,聚焦隐匿性脑血管损伤的基层适宜性筛查瓶颈和挑战,实现对无症状性脑梗死的自动识别及未来卒中风险的精准分层预测。该系统性能的泛化性通过在新加坡、马来西亚、美国、英国、丹麦及中国香港等多地临床队列的广泛验证,证实该创新性技术可有效识别SBI和未来卒中风险,通过更简单、实用和具有成本效益的方法提高卒中风险预测的准确性,为卒中预防管理提供新策略。

图1. DeepRETStroke系统研究成果2025年6月在线发表于Nature Biomedical Engineering
从糖尿病大血管病变到“无声脑梗”——亟须早识别、早干预的卒中风险隐患
脑卒中是全球死亡和长期残疾的主要原因之一,也是糖尿病患者常见的大血管并发症之一,而其中“无症状性脑梗死”(SBI)更是广泛存在却难以被发现的“隐匿杀手”。数据显示,一般人群中SBI患病率高达20%,在糖尿病患者中更甚。SBI的发生常无明显临床症状,但显著增加未来脑卒中、痴呆及死亡的风险。据文献报道,我国40岁及以上人群脑卒中现患人数达1242万,且发病人群呈年轻化。平均每10秒就有1人初发或复发脑卒中;在脑卒中幸存者中,约75%人群留有不同程度的后遗症,这进一步强调了脑卒中筛查和预防的紧迫性。然而,当前SBI和脑卒中的发现仍高度依赖昂贵且有限可及的脑影像技术(如MRI),使得广泛筛查面临现实瓶颈。
视网膜作为中枢神经系统的延伸部分,因其能够作为观察脑部血管与神经健康状况的独特窗口,一直备受神经科学、脑科学等多学科领域的关注。研究团队通过医工交叉合作,受“眼-脑连接”概念的启发,创造性地利用深度学习方法构建了全球首个眼-脑轴影像基座模型,并在此基础上开发了DeepRETStroke深度学习系统。该系统能够通过眼底图像这一简便、无创且易于获取的媒介,实现对SBI和卒中风险的智能识别与预测:其一,利用DeepRETStroke系统从视网膜图像中检测SBI;其二,借助视网膜检测到的SBI特征来优化未来卒中风险预测,并微调模型以预测卒中复发。

图2.眼-脑轴垂域基座模型赋能DeepRETStroke系统,实现无症状脑梗便捷筛查
创新跨器官影像预训练策略,打造全球首个眼-脑轴跨器官垂域基座模型
研究团队构建了三阶段跨器官影像预训练策略,实现眼-脑垂域基座模型的构建。第一阶段:通过无监督学习增强模型跨种族泛化能力,训练数据来自中国两大队列超80万的视网膜图像;第二阶段:通过监督学习初始化基座模型并建立“眼-脑关联”先验知识,提高后续模型学习的稳定性和可靠性。第三阶段:通过半监督学习和知识迁移强化基座模型,采用无卒中病史的大规模数据集和具备脑影像诊断“金标准”的数据集相结合的开发框架,进一步优化模型对“眼-脑关联”特征的表示能力,提升模型对无症状性脑梗死(SBI)检测和卒中预测的表示能力。通过上述三步预训练策略,成功创建了眼-脑轴特定垂域的跨器官影像基座模型,并在马来西亚、新加坡、美国、英国、丹麦及中国香港等多个人群队列的20万张眼底图像和临床数据中进一步验证。DeepRETStroke系统可无创识别既往未被诊断的SBI,同时还可预测未来5年首次脑卒中及卒中复发的风险,显著优于传统基于年龄、血压等临床指标的预测模型,并且在不同人种中具有较好的鲁棒性和泛化性。值得一提的是,在对218名脑卒中患者的前瞻性干预研究中,与临床数据模型相比,DeepRETStroke基于眼底图像进行风险分层,对高危组给予多维度强化干预(健康管理、血压控制、代谢指标改善等),显著降低了卒中复发风险,这表明DeepRETStroke系统在指导卒中复发预防策略方面具有巨大的临床应用潜力。
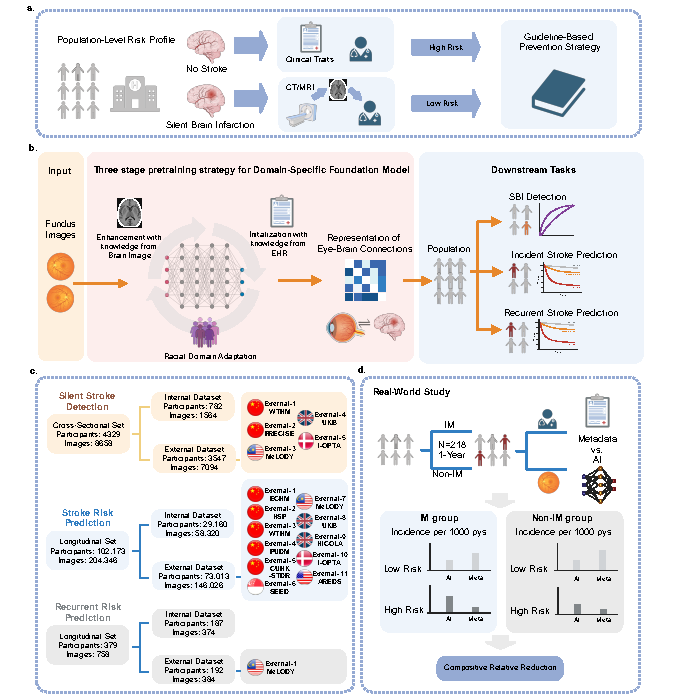
图3. DeepRETStroke系统:眼-脑轴跨器官影像基座模型研究设计
打造人群卒中防控新路径,推动AI辅助脑健康管理落地应用
DeepRETStroke系统的构建突破了卒中早期筛查对高成本脑影像技术的依赖,填补了卒中前“无声阶段”识别的技术空白,有望为高风险人群管理提供普惠化、可推广的解决方案。其在无需高端设备的条件下,仅通过一次眼底照相,即可完成对脑部微梗死的“窥见”与未来卒中风险的量化评估,还为个性化预防策略提供了可操作的见解,适用于糖尿病等高危人群的常规筛查和基层医疗场景。
通过基于人工智能的不断创新与持续突破,DeepRETStroke为构建“眼底—脑部—卒中”的AI预警生态系统奠定了坚实基础。未来,研究团队将着力推动DeepRETStroke系统的临床应用与转化,并积极探索其在更广泛的神经系统疾病中的潜在应用场景。通过AI创新赋能眼-脑健康窗口,DeepRETStroke能够释放视网膜中蕴含的“脑信号”,有望成为新时代神经系统疾病管理的预警先锋。
作者信息
上海交通大学计算机学院博士生姜楠(导师盛斌教授)、清华大学医学院博士后纪宏伟(导师黄天荫教授)、上海交通大学医学院博士生管洲榆(导师贾伟平教授)、北京天坛医院研究员潘岳松、华中科技大学附属同济医院博士生邓晨心(导师张存泰教授)、清华大学郭雨晨研究员(戴琼海教授团队)、上海交通大学医学院附属第六人民医院博士后刘丹(导师贾伟平教授)以及上海市保健医疗中心陈婷丽主任为本文共同第一作者。本工作还得到了来自国家基层糖尿病防治管理办公室、华中科技大学、北京协和医院、北京同仁医院、中山大学中山眼科中心、香港中文大学等多个机构及专家团队的支持和帮助。此外,新加坡、美国、英国、丹麦及马来西亚等国的多学科专家团队给予了帮助和支持。该研究得到科技部国家重点研发计划、国家自然科学基金、北京市自然科学基金和上海市科委“一带一路”国际联合实验室建设项目等资助。DeepRETStroke系统及眼-脑垂域基座模型研发所需计算资源受到上海交通大学“交我算”计算平台和上海交通大学AI for Science科学数据开源开放平台的支持。
论文链接:https://www.nature.com/articles/s41551-025-01413-9