
 探索发现 · 交大智慧
探索发现 · 交大智慧
上海交大万兵兵课题组发表酵母DNA损伤检验点调控新机制的研究论文
2025年1月2日,上海交通大学系统生物医学研究院万兵兵课题组与纽约MSKCC癌症研究中心Xiaolan Zhao教授团队合作于Nature子刊Nature Communications杂志上在线发表了题为Mms22-Rtt107 axis attenuates the DNA damage checkpoint and the stability of the Rad9 checkpoint mediator的研究论文,揭示了酵母Mms22蛋白调控DNA损伤检验点的分子机制。因为从酵母到人这一DNA损伤检验点的调控机制高度保守,这一新发现为与DNA损伤检验点密切相关的人类肿瘤发生发展的机制研究和未来可能的诊断与治疗提供了新的线索。

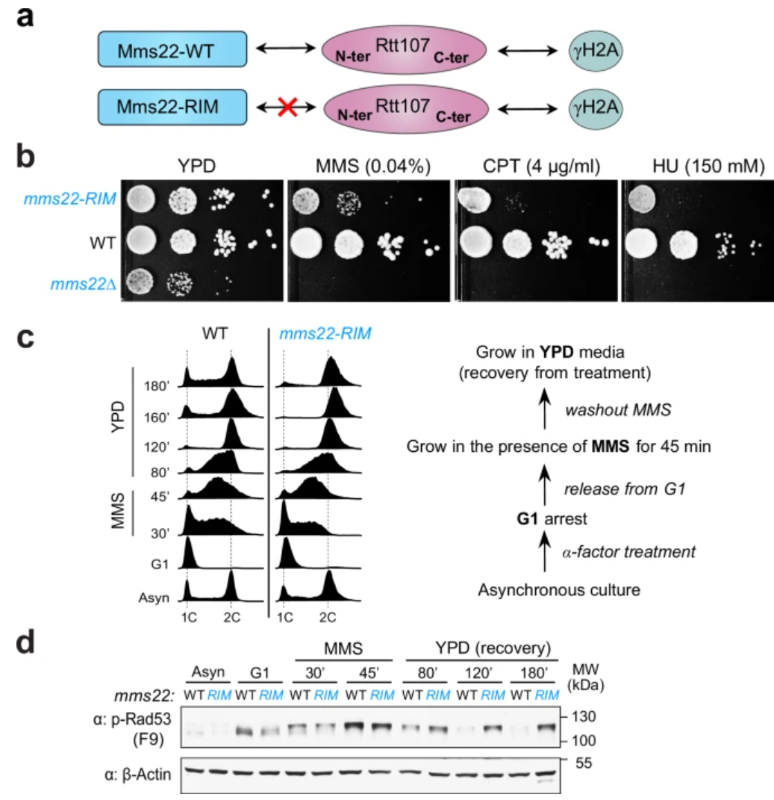
该研究先以分子遗传学为研究方法,发现破坏了Mms22蛋白与Rtt107蛋白的点突变体Mms22RIM对遗传毒性药物MMS, CPT和HU等过度敏感以及其造成了DNA损伤检查点的持续激活。
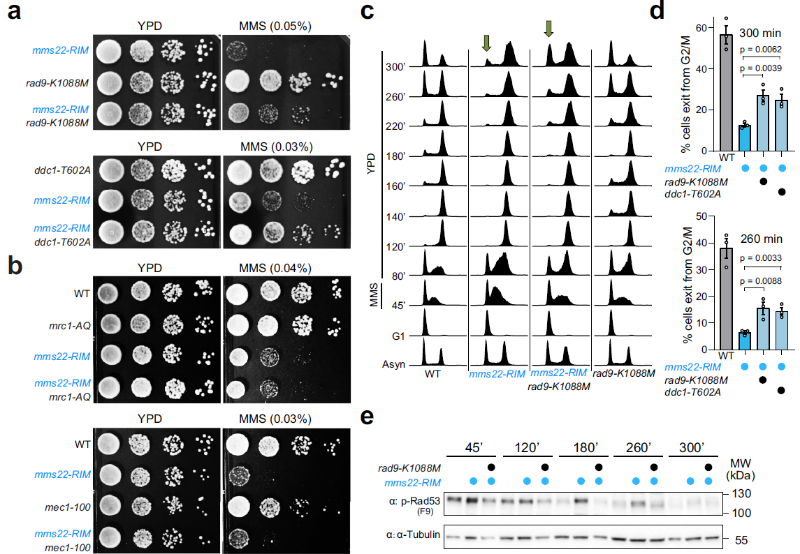
随后他们通过酵母点板实验发现DNA 损伤检查点蛋白的轻微突变(rad9-KM和ddc1-TA)等位基因可挽救 mms22RIM细胞的生长、细胞周期控制以及DNA损伤响应效应激酶Rad53的活化等相关表型。
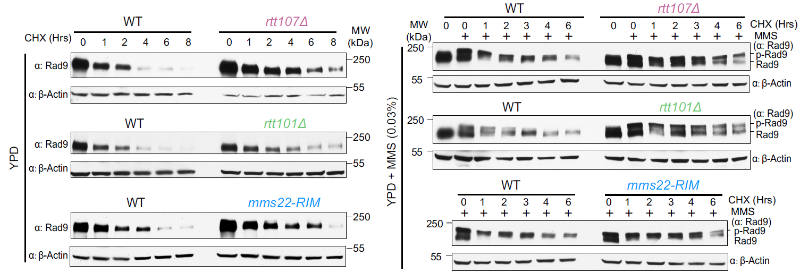
接下来的研究他们发现DNA损伤响应效应激酶Rad53上游的介导蛋白Rad9的蛋白量受Rtt101Mms1 泛素连接酶E3的调控,Mms22的点突变体Mms22RIM对导致Rad9蛋白量的增加。
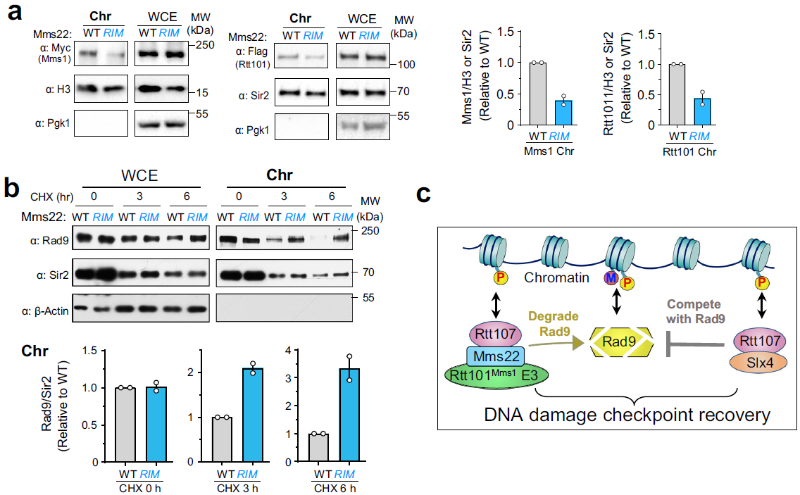
最后通过细胞染色质组分分离实验,他们发现Rtt101Mms1泛素连接酶E3是通过和Mms22-Rtt107蛋白复合体的相互作用被招募到染色质上去,从而通过蛋白酶体降解染色质结合的 DNA损伤响应调控蛋白Rad9 的。这一发现是该领域在2013年发现Slx4通过和Rtt107结合减弱DNA损伤检查点之后的又一重要进展。
上海交通大学系统生物医学研究院基因组不稳定性与肿瘤相关性研究课题组万兵兵研究员与纽约MSKCC癌症研究中心Xiaolan Zhao教授为本文的共同通讯作者。上海交通大学系统生物医学研究院为第一作者单位。该研究得到国家自然科学基金(32170087)、转化医学国家重大科技基础设施(上海)开放课题等项目的资助。
论文链接:https://www.nature.com/articles/s41467-024-54624-0