
 探索发现 · 交大智慧
探索发现 · 交大智慧
结构重排驱动生物合成
上海交大邓子新团队揭示二聚化非核糖体肽合成酶的催化循环轨迹
近日,上海交通大学生命科学技术学院、微生物代谢国家重点实验室邓子新教授团队于《自然通讯》(Nature Communications)杂志上发表题为 “表异构酶嵌入式二聚化非核糖体肽合成酶的催化轨迹”(Catalytic trajectory of a dimeric nonribosomal peptide synthetase subunit with an inserted epimerase domain)的研究论文。该工作通过结构生物学与生物化学相结合的手段,解析致病因子合成机器多个催化状态的三维结构,捕获其连续催化循环轨迹,深入推动次生代谢巨型合酶的结构研究,为理解二聚化非核糖体肽合成酶的催化机理、衍生新型靶点抑制剂药物提供蛋白结构基础。上海交通大学博士后王嘉良与硕士生李丹丹为该论文共同第一作者,邓子新教授、梁晶丹副研究员和汪志军副研究员为共同通讯作者。
非核糖体肽合成酶(NRPSs)是一类多结构域、模块式巨型合酶,能够合成具有广泛生物活性的天然产物,从临床用药(抗生素、抗肿瘤抑制剂以及免疫抑制剂等)到致病因子(致癌分子、铁载体等)。NRPSs以“装配线”的方式进行催化,其中的延伸模块催化以下步骤:底物激活、中间产物穿梭以及缩合反应;有时,还可催化修饰性的表异构化反应。
然而,高分辨NRPSs延伸模块结构信息的缺乏,障碍了人们进一步理解该类巨型合酶的催化机制。例如,NRPSs中的关键结构域、氨基酸如何进行底物的识别、激活与延伸?修饰性结构域嵌入全酶的组织构架怎样?完整的巨型合酶如何通过关键性结构域的移动进行终产物的合成?自身各个结构域间如何动态协调完成催化循环?
针对上述关键性问题,邓子新教授团队通过冷冻电子显微镜单颗粒分析技术,成功解析2.97 Å、3.78 Å和3.47 Å的一个典型NRPS延伸模块PchE的三个高分辨构象(图1)。该巨型合酶负责铜绿假单胞菌中致病因子Pyochelin的生物合成,包含五个催化结构域,分别为:芳香基载体蛋白(ArCP)、缩合环化结构域(Cy)、腺苷化结构域(A)、表异构酶(E)以及肽基载体蛋白(PCP)。作为罕见的二聚化NRPS,PchE呈现一种特殊的头对尾、“H” 形构架。二聚化界面完全由两个单体中Cy-A结构域的反向相互作用介导,互作面积达到2337 Å2。
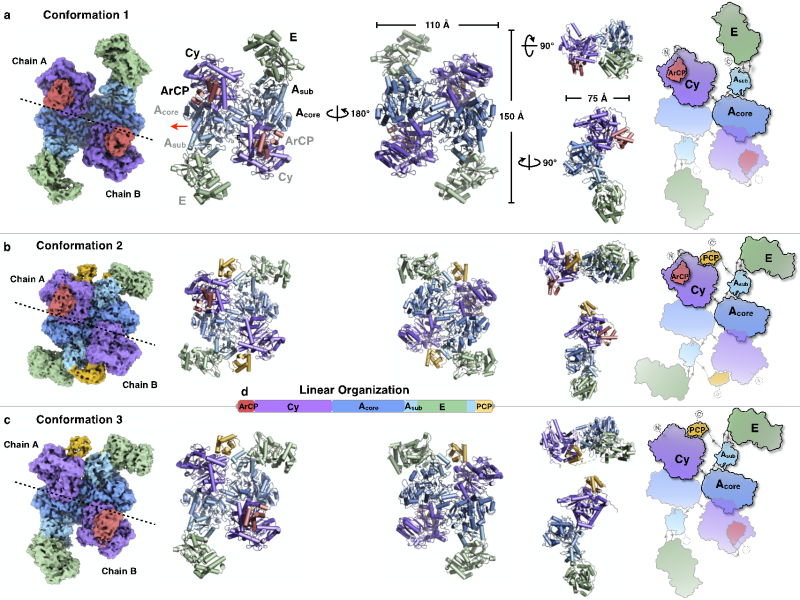
图1.PchE三个构象的构架
PchE的三个构象对应了三种不同的催化状态:底物供给、缩合以及缩合后构象。三者的分别捕获明确了Cy结构域与两个载体蛋白的结合模式;建立了底物、终产物与底物通道、活性位点之间的相互作用关系(图2)。在结构信息指导下,通过对关键活性位点氨基酸的点突变与生化检测,阐明其环化缩合过程中关键氨基酸对线性中间产物生成的影响以及环化终产物合成的原理。在催化过程中,Cy结构域中氨基酸F372的旋转起到开关控制作用(视频1)。当其芳香环侧链朝向外侧时,ArCP能够与Cy结构域结合,通过磷酸泛酰化巯基乙胺手臂供给小分子水杨酸底物;反之当芳香环侧链旋转至内侧时,底物通道被截断,ArCP无法供给底物。
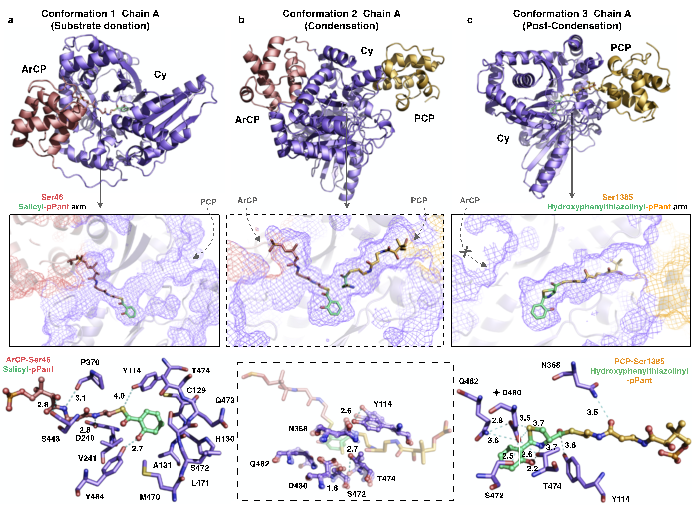
图2.Cy结构域的底物供给、缩合及缩合后催化状态
利用神经网络深度学习的手段,研究人员进一步观察到PchE完整催化循环的连续动态轨迹,从底物激活直至表异构化反应(图3,视频2)。催化反应起始于构象(i),ArCP结合在Cy结构域上,代表底物供给构象。(ii)随后PCP移动至处于硫酯形成构象的A结构域,加载被激活的底物L型半胱氨酸。(iii)此时,A羧基末端亚结构域,连带镶嵌式E结构域发生约155° 的大尺度旋转,从硫酯形成构象转变为腺苷形成构象,准备加载、激活下一分子半胱氨酸。(iv)接近着,PCP与ArCP同时结合在Cy结构域的两侧并分别供给底物水杨酸与半胱氨酸,Cy结构域催化两个底物分子的缩合、环化。(ⅴ)随后ArCP结构域离开Cy,推测其与上游激活模块相互作用并加载新一个水杨酸底物分子。(ⅵ)最终,A羧基末端亚结构域重新旋转回来,再次呈现硫酯形成构象;PCP携带缩合环化后的中间产物移动至E结构域,后者将二氢噻唑环部分的立体异构从L型转换为D型。在将中间产物传递至下游蛋白模块后,PCP重新恢复(i)的位置,准备开启下一轮的催化循环。
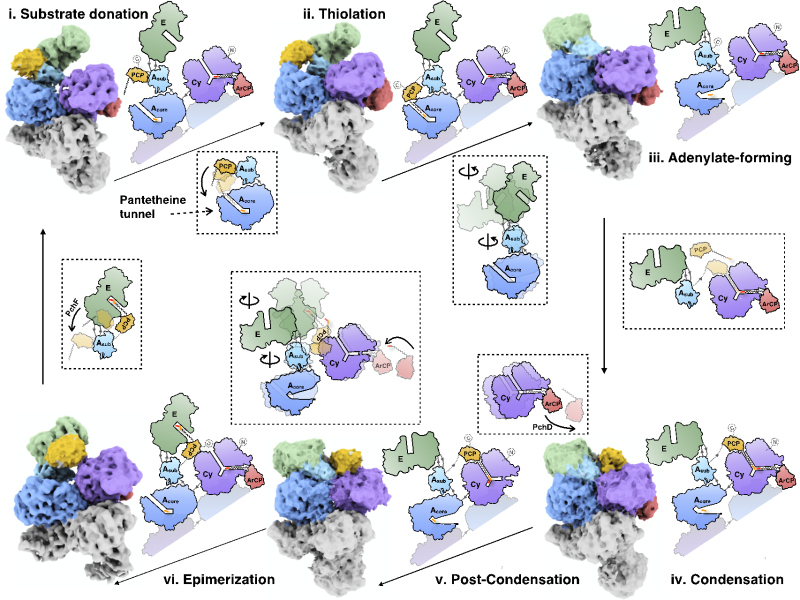
图3.PchE的催化循环轨迹
综上所述,典型的NRPS延伸模块PchE,通过整合多个维度下的结构重排,驱动终产物的合成,犹如一场精心设计的生物大分子舞蹈。结构域的大尺度移动造就不同的催化状态,底物通道的开关控制小分子化合物的进入与否,关键氨基酸的位置协调催化反应的进行。该结构的解析建立了模块内、结构域间催化轨迹的基本框架,为工程化改造修饰性结构域嵌入式的二聚化NRPSs,合成创新药物提供结构基础。
英国剑桥大学医学研究所(CIMR) Tristan Croll副研究员、上海交大博士生曹卫、硕士生陈璐、生科院仪器平台张薇老师、国家蛋白质科学中心(上海)孔亮亮老师参与了该项工作。
感谢国家蛋白质中心王芳芳、辛立辉、李光一、段佳琳、刘娜等老师的技术支持。感谢上海交通大学超算中心π 2.0集群以及孙锦文老师提供的平台及技术支持。 感谢中国科学院分子植物科学卓越创新中心尤琳琳博士以及麻省理工学院(MIT)Ellen D. Zhong博士的帮助。
该研究得到了国家重点基础研究发展计划合成生物学专项(2018YFA0900700、2019YFA0905400、2021YFA0910500)、国家自然科学基金(32171252、91753123、31470830)、上海超级博士后激励计划(202112)以及Wellcome Trust(209407/Z/17/Z)的经费支持。
视频1链接:https://life.sjtu.edu.cn/Assets/userfiles/files/Supplementary%20Movie%201.mp4(F372控制Cy结构域底物通道的开放与关闭)
视频2链接:https://life.sjtu.edu.cn/Assets/userfiles/files/movie2(1).mp4(PchE催化轨迹的连续动态过程)
文章链接: https://www.nature.com/articles/s41467-022-28284-x