
 探索发现 · 交大智慧
探索发现 · 交大智慧
上海交大生科院林双君团队ACS Catalysis发文:“一锅酶法”制备氟苯尼考合成的最直接手性中间体
近日,国际知名期刊《ACS Catalysis》在线发表了生命科学技术学院林双君团队的研究成果“One-Pot Asymmetric Synthesis of an Aminodiol Intermediate of Florfenicol Using Engineered Transketolase and Transaminase”。林双君教授为通讯作者,生命科学技术学院研究生刘琦为第一作者。

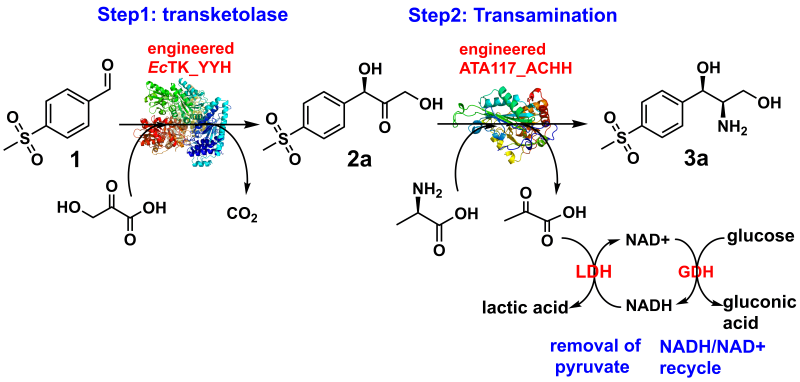
在对转酮酶和转氨酶催化机制和蛋白结构认识基础上,利用分子对接手段建立了酶-底物结合模型,并基于此设计半理性突变策略,翻转了转酮酶的立体选择性,转氨酶的对映体偏好性和醛酮选择性,进而偶联转酮酶和转氨酶突变体一锅法合成了末端羟基手性中间体(1R,2R)-对甲磺砜基苯丝氨醇,产率可以达到76%,非对映体选择性最高为96% de 和对映体选择性>99% ee,为氟苯尼考的制备提供了最直接的手性中间体。
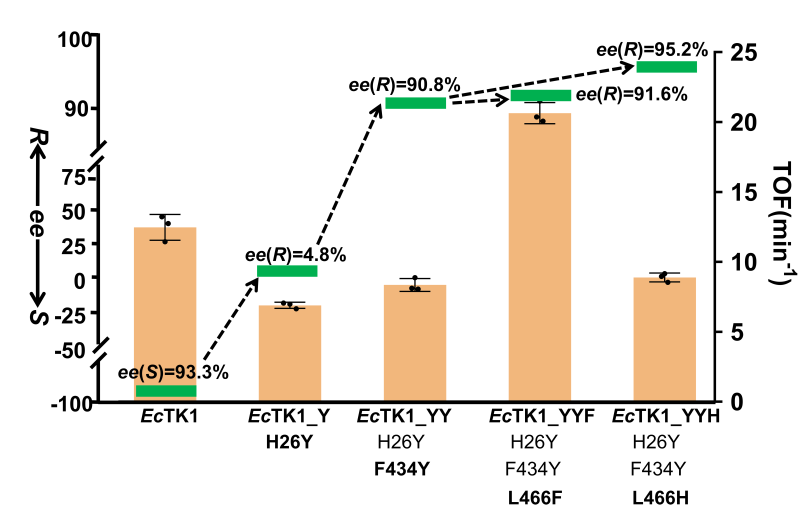
转酮酶EcTK1的蛋白质进化
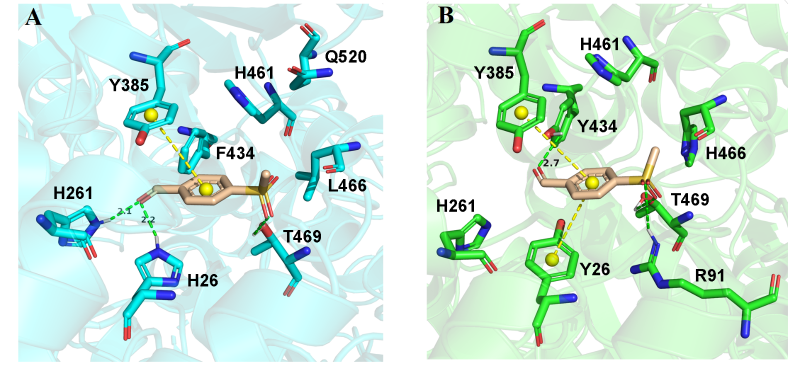
转酮酶EcTK1 (A)和EcTK1_YYH (B)与醛1的分子对接
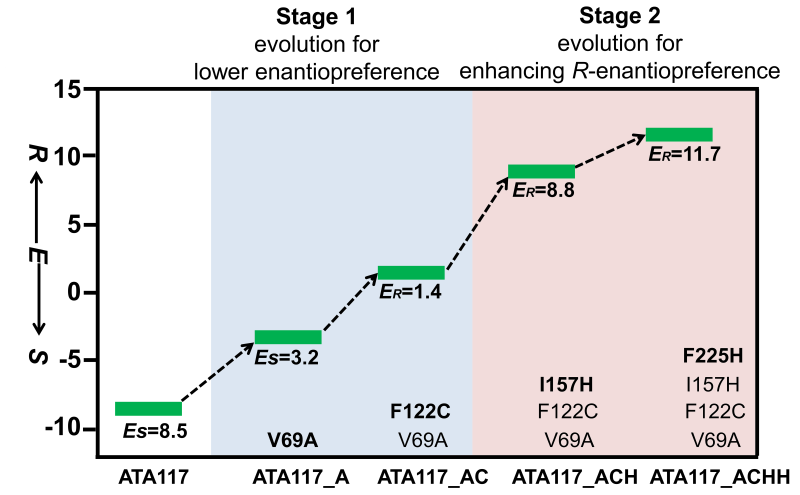
转氨酶ATA117的蛋白质进化
基于设计,研究者从一系列转酮酶和转氨酶中筛选出能有效催化起始底物醛1的转酮酶突变体EcTK1和有效催化转酮酶产物2氨基化的ω-转氨酶ATA117。为了考察转酮酶的立体选择性,建立了一个通过非手性液相测定2立体构型的方法,即偶联一个对2基本无立体选择性的R-转氨酶突变体ATA117_AC,将(S)-和(R)-2分别转化成(1S,2R)-和(1R,2R)-3。从而可以确定EcTK1是S-选择性的,催化产生的羟酮中间体为S-构型(93.3% ee)(如图1所示)。由于所设计的路线是合成R-羟酮中间体,因此基于转酮酶的蛋白质结构和催化机制对该酶作了半理性改造。首先将底物醛1对接进EcTK1晶体结构的活性口袋中 (如图2A所示),发现醛羰基与H26和H261存在氢键相互作用,而F434位于醛羰基的背面。因此提出一个假设,如果通过氨基酸突变改变醛羰基的定位,那么很有可能会改变羟酮产物的立体构型。为了翻转醛羰基的朝向,采用了“破而后立”的策略,即先打破现有的氢键相互作用,而后建立新的氢键相互作用。通过迭代的饱和突变和理性突变,获得了立体选择性完全翻转的EcTK1_YYF和EcTK1_YYH突变体,ee(R)分别为91.6%和95.2% (如图1所示)。通过将突变体EcTK1_YYH与底物醛1进行分子对接,证实了醛羰基的朝向的确发生了翻转,与背面的Y434形成了新的氢键(如图2B所示)。
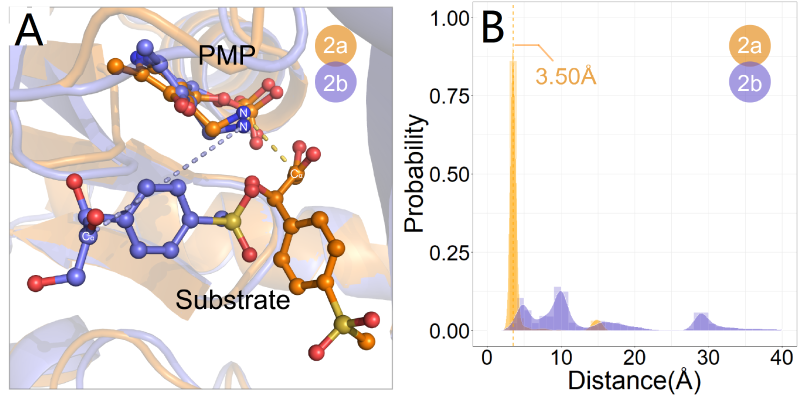
分子动力学数据的统计
在实现转酮酶的立体选择性翻转后,作者基于R-2底物与ATA117_AC的分子对接,对转氨酶作了迭代饱和突变,筛选所得突变体ATA117_ACHH翻转了对手性羟酮中间体2的对映体偏好性和醛酮底物选择性,即从野生型ATA117对S-酮的偏好性(Es=8.5)翻转为突变体ATA117_ACHH对R-酮的偏好性(ER=11.7) (如图3所示);从野生型ATA117对醛的偏好性翻转为突变体ATA117_ACHH对酮的偏好性。为了考察ATA117_ACHH对R-酮的偏好性,分别作了ATA117_ACHH与-S酮2b和R-酮2a的分子动力学模拟,证实氨基供体PMP的氨基与R-酮的羰基距离在3.5Å左右,而与S-酮羰基距离为10-30Å (如图4所示)。
在获得了合适的转酮酶和转氨酶突变体之后,将两个酶偶联一锅反应合成了目标产物氟苯尼考手性中间体(1R,2R)-对甲磺砜基苯丝氨醇,产率为76%,非对映选择性为96% de和对映选择性> 99% ee,并且进一步将该级联反应拓展到其他一系列对位取代的苯甲醛,合成了相应的(1R,2R)-对位取代的苯丝氨醇衍生物,产率为51-80%,de为95-97%。
该研究工作得到了国家重点研发计划项目(2018YFA0901900)和国家自然科学基金项目(21632007,31425001)的资助。
论文链接:https://pubs.acs.org/doi/10.1021/acscatal.1c01229