
 探索发现 · 交大智慧
探索发现 · 交大智慧
上海交通大学系统生物医学研究院陶生策团队揭示新型冠状病毒(SARS-CoV-2)Orf9b抑制一型干扰素应答机制
COVID-19的大流行正威胁着全球亿万民众的健康。到目前为止,仍然没有针对SARS-CoV-2的“特效药”。为了加速药物开发,迫切需要鉴定关键性的分子靶标以及它们在感染过程中发挥的角色。一型干扰素(IFN-I)应答是免疫系统抵御病毒侵染的中心事件. 近期多篇研究表明与其他病毒相比,SARS-CoV-2最突出的特征是其在病人体内尤其是重症患者体内能强烈抑制IFN-I的产生1,2。此外也有研究发现利用甘草甙模拟IFN-I能有效的阻止SARS-CoV-2的感染3。因此,解析SARS-CoV-2如何抑制IFN-I应答可为设计COVID-19治疗策略提供重要思路。
2020年7月29日,上海交通大学陶生策团队在Cellular & Molecular Immunology上发布了SARS-CoV-2 Orf9b通过结合TOM70抑制一型干扰素应答的文章: SARS-CoV-2 Orf9b Suppresses Type I Interferon Responses by Targeting TOM70。

该团队之前利用SARS-CoV-2蛋白质组芯片发现除了S蛋白和N蛋白,Orf9b在COVID-19康复病人中也有较强的免疫应答反应(Bioart 链接 https://mp.weixin.qq.com/s/6cjM2irUKQKbmUH8-T1_yg)。因此推测Orf9b可能具有重要的生理或病理作用。在此项研究中,该团队首先通过亲和质谱实验获取Orf9b的相互作用蛋白谱,进一步的实验揭示SARS-CoV-2的Orf9b和线粒体外膜蛋白受体同时也是IFN-I应答通路组分蛋白TOM70存在直接的强相互作用(Kd = 44.9 nM)。同时发现类似的结合强度也存在于SARS-CoV的Orf9b和TOM70之间。生化实验揭示TOM70的受体结合区域对其与Orf9b的结合至关重要。荧光共聚焦实验揭示SARS-CoV/SARS-CoV-2的Orf9b和TOM70均共定位在线粒体外膜上。功能实验发现Orf9b能够显著的抑制细胞内IFN-I的产生,并且TOM70的过表达在很大程度上能抵消Orf9b介导的对IFN-I的抑制。
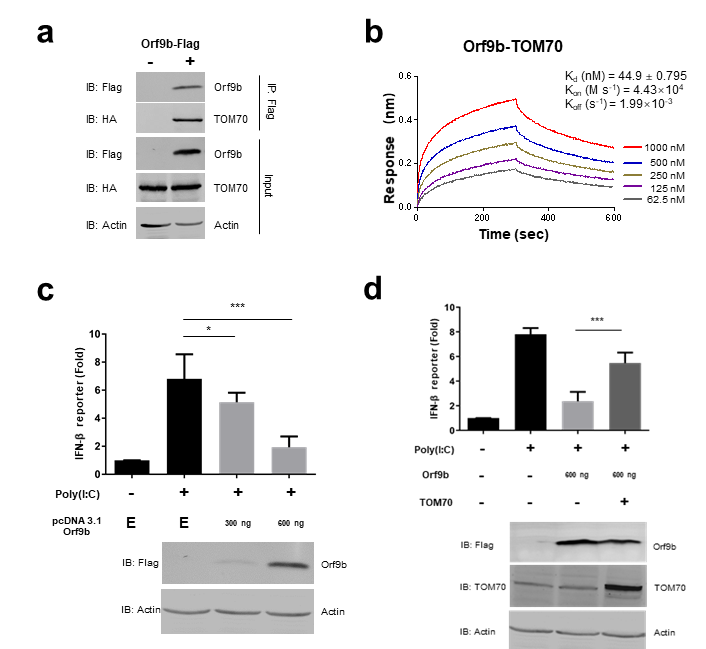
图一 a. Orf9b免疫共沉淀TOM70 b. BLI测定Orf9b与TOM70亲和力
c-d. 检测Orf9b在HEK293T 细胞或 TOM70过表达情况下对IFN-I表达的影响
考虑到IFN-I在人体抗病毒应答过程中的关键作用,在COVID-19病人体内恢复IFN-I应答可能是一个潜在治疗选项。此项研究提供了一种潜在的药物设计方案,即通过开发针对Orf9b和TOM70相互作用界面的抑制剂恢复IFN-I的应答来治疗COVID-19。同时由于SARS-CoV 的Orf9b与TOM70也有比较强的亲和力,同样的策略也许可以应用到SARS的治疗中。此外,TOM70除了在一型干扰素通路发挥作用之外,在心肌细胞、神经细胞等中也是一个重要的分子开关。本项研究为新冠引起的相关器官紊乱提供了一个可能的机制解释。
本项研究的共同第一作者为上海交通大学博士江何伟,博士张海南,博士孟庆峰和博士谢佳,通讯作者为上海交通大学研究员陶生策。
1. Blanco Melo D, Nilsson Payant BE, Liu WC, et al. Imbalanced Host Response to 176 SARS-CoV-2 Drives Development of COVID-19. Cell 2020; 181: 1036-1045 e1039.
2. Jérôme Hadjadj et al. Impaired type I interferon activity and inflammatory responses in severe COVID-19 patients. Science, 2020, doi:10.1126/science.abc6027.
3. Zhu J, Deng YQ, Wang X, et al. An artificial intelligence system reveals liquiritin inhibits SARSCoV-2 by mimicking type I interferon. bioRxiv 2020, doi: https://doi.org/10.1101/2020.05.02.074021
文章链接:
https://www.nature.com/articles/s41423-020-0514-8