
 探索发现 · 交大智慧
探索发现 · 交大智慧
上海交通大学高维强、李力组发现:Di-Ras2——肾癌中一个连接VHL介导泛素化与MAPK通路的新桥梁
肾透明细胞癌(ccRCC)是世界上最常见、最致命的泌尿系恶性肿瘤之一。Ras家族是一类小GTPases,在包括ccRCC在内的许多疾病中起着“分子开关”的作用,是ccRCC的病理驱动因素之一。其中,DIRAS2基因编码的GTPase与Ras和Rap有60%的同源性,并且在ccRCC中的表达水平明显要高于正常肾脏。同时,von Hippel-Lindau(VHL)是一个在ccRCC中频繁丢失或突变的基因,也是ccRCC形成和发展的最重要基因之一。

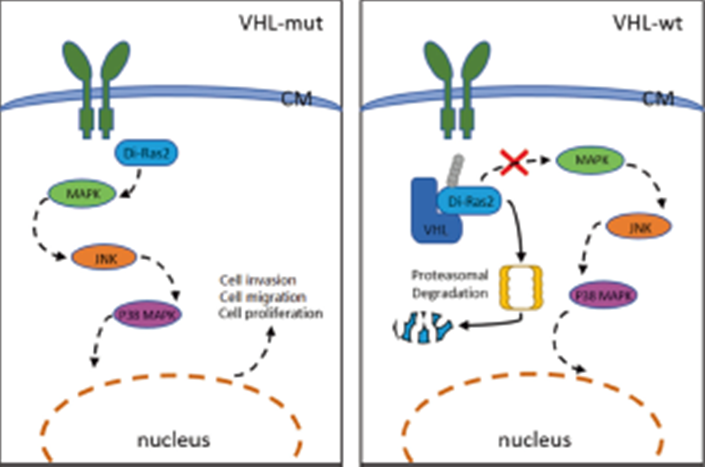
上海交通大学生物医学工程学院高维强,李力课题组于2020年2月25日在Nature旗下肿瘤学期刊Oncogene上在线发表了研究成果“Di-Ras2 promotes renal cell carcinoma formation by activating the mitogen-activated protein kinase pathway in the absence of von Hippel–Lindau protein”,并受邀为Nature Research Cancer Community site撰写评述“Behind the paper: Di-Ras2, a potential oncogene associated with the crosstalk between VHL-mediated ubiquitination and the MAPK pathway in ccRCC”。该项研究继续探索了潜在的癌基因产物Di-Ras2促进ccRCC进展的分子机制。研究者发现Di-Ras2在ccRCC中上调,在VHL蛋白(pVHL)缺失的情况下,促进了人肾癌细胞的增殖、迁移和侵袭。进一步的机制探索表明,Di-Ras2通过调节下游效应分子的磷酸化,激活Ras/MAPK信号通路,从而促进ccRCC的形成。针对Di-Ras2和pVHL潜在的相互作用机制,研究者首次报道了E3泛素连接酶pVHL可以作用于Di-Ras2并促进其泛素化和降解,从而抑制Di-Ras2的促肿瘤功能。这些结果表明Di-Ras2可以在VHL缺陷的条件下促进ccRCC的发生,这为进一步研究pVHL与MAPK通路在ccRCC肿瘤发生中的关系提供了新的视角。Di-Ras2也可能成为一个新的肾癌诊断标志物和治疗的药物靶点。
饶汉钰博士生、李雪峰博士是论文的第一作者。高维强教授和李力副研究员是论文的通讯作者。该项研究得到了来自科技部国家重点研发计划、国家自然科学基金委、上海市科委及王宽诚基金会等资助。该研究也得到了上海市教育委员会高峰高原学科建设计划的支持。
原文链接:https://www.nature.com/articles/s41388-020-1247-y