
 探索发现 · 交大智慧
探索发现 · 交大智慧
上海交大洪亮课题组与合作者:热力学基本概念助力耐高温蛋白的理性设计
2018年10月,上海交通大学物理与天文学院、自然科学研究院洪亮特别研究员课题组与美国田纳西大学生物化学和分子生物学系副教授Nitin Jain课题组合作,在《美国科学院院报》(Proceedings of the National Academy of Sciences of the United States of America,简称PNAS) 上发表探索嗜热细胞色素蛋白热稳定性机理的研究文章(Entropic Contribution to Enhanced Thermal Stability in the Thermostable P450 CYP119, Proc. Natl. Acad. Sci. USA, 2018)。该工作发现嗜热细胞色素蛋白由于其在自然折叠态较高的柔性,减小解折叠过程中熵的驱动力,获得耐高温的能力。这一发现为耐热蛋白的理性设计提供了从熵出发的全新思路。
细胞色素P450是一种普遍存在于细菌,动物及人体内的一类亚铁血红素蛋白,在药物代谢与排毒方面有着重要的作用,并协助人体合成包括胆固醇和类固醇在内的许多生命所必需的物质。然而,蛋白质大分子一般都不耐高温(~50°C解折叠),这限制了其在高效的酶工程及严苛的机理研究中的应用。因此,如何提高蛋白的热稳定性成为了科学研究和工业生产所共同关注的问题。从热力学基本概念出发,提高蛋白质热稳定性,等价于增加其解折叠的自由能能垒(G)。此能垒包含了焓与熵两个部分。一方面:蛋白质在自然的折叠状态下会形成多种多样残基间的相互作用,比如氢键,盐桥,疏水相互作用等等。这些相互作用(即焓的作用)是帮助蛋白抵抗环境变化(例如升温,加压等),保持自然折叠态的正能量。另一方面:蛋白质解折叠过程中其结构上无序度会明显升高,即熵的增加,这无疑是驱动蛋白质解折叠的内在动力。当前流行的提高蛋白质热稳定性的酶工程设计思路往往是从焓的角度出发,即通过突变某些蛋白质残基引入较强的残基间相互作用,例如氢键,盐桥等。这种做法虽然能增加蛋白质解折叠的能垒,提高其解折叠温度,但往往造成蛋白质分子的刚性,降低其柔软度,进而牺牲其反应活性。如何有效提高生物酶的热稳定性,又能增加或者不降低其生物活性是酶工程学的重要课题。
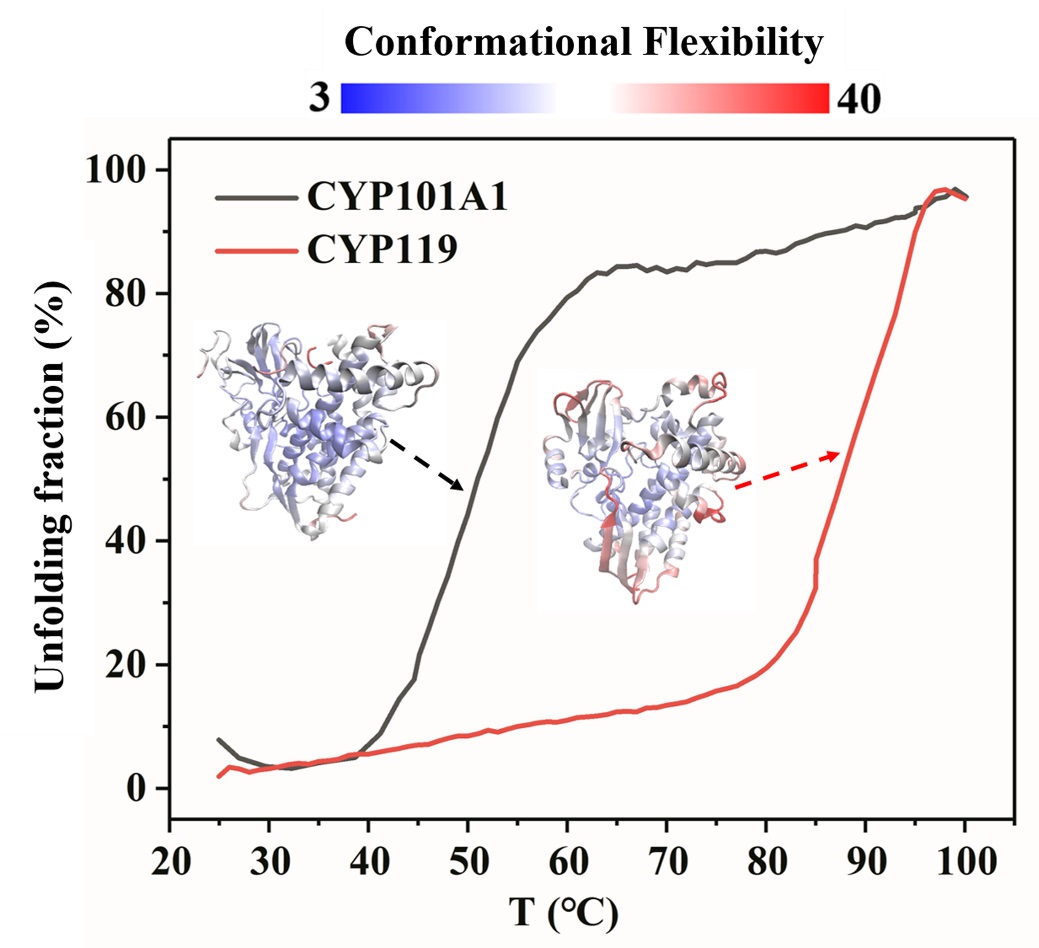
在研究细胞色素P450蛋白质家族时,洪亮课题组及其合作者选取热稳定性高的嗜热蛋白CYP119与同家族的常规蛋白CYP101A1进行对比研究。通过使用中子散射与核磁共振谱实验对蛋白的动力学进行表征,他们发现在相同温度下,嗜热蛋白CYP119比常温蛋白CYP101A1具有更高的结构柔性。换句话说,CYP119不仅耐高温,而且更活跃。这一反直觉的实验结果预示着必然有不同于常规的热稳定性机理在起作用。该团队通过圆二色谱以及荧光光谱定量测量了这两种蛋白在广阔的温度区间的解折叠自由能能垒,并分解出焓与熵两个部分各自的贡献。结果表明,单从焓的角度出发,CYP119其实更不稳定,因为其焓的能垒更小。它之所以能耐高温是由于这个蛋白在解折叠过程中熵的增量非常小,即蛋白质解折叠的“内在动力“不足。通过深入分析动力学的实验数据,该团队发现导致CYP119解折叠的熵变小的一个重要原因是其在自然折叠态的时候柔性非常高,换言之它在折叠态的熵已经很大,没有多大动力去解折叠。不同于常规的“高焓”机理,本研究发现折叠态柔性强这种“高熵”状态可以降低蛋白解折叠过程中熵的驱动力,从而使得蛋白质耐高温。另外,“高熵”状态还将有助于提高酶的生物活性,比如结合更多种类的底物,更高催化效率等。本研究成果为将来设计新型耐热蛋白提供了全新的思路,即通过突变某些残基制备折叠态柔性强的蛋白,它有可能既具备耐热性又有高活性的特征。
此项目受到国家自然科学基金(11504231和31630002)以及中组部青年千人计划的支持。文章的第一作者是上海交通大学物理天文学院、自然科学研究院洪亮课题组博士生刘卓,洪亮特别研究员和田纳西大学Nitin Jain教授为本文的共同通讯作者。中子散射和圆二色谱测量由洪亮课题组完成,核磁共振和荧光光谱测量由Nitin Jain教授课题组承担。
论文链接:http://www.pnas.org/content/early/2018/10/04/1807473115.full