
 探索发现 · 交大智慧
探索发现 · 交大智慧
交大团队揭示核PTEN发挥肿瘤抑制作用新机制:调控RNA剪接影响高尔基体
近日,上海交通大学医学院细胞分化和凋亡教育部重点实验室在《Nature Communication》报告存在于细胞核内的PTEN蛋白通过与mRNA剪接体相互作用,调控前体mRNA(pre-mRNA)的可变剪接,进而干预高尔基体的伸展和分泌,发挥其肿瘤抑制作用。
PTEN是最重要的肿瘤抑制基因之一。广为人知的是,它通过脂质磷酸酶功能抑制磷脂酰肌醇3-激酶的酶活。然而,新近研究表明,缺失磷酸酶活性的PTEN突变体仍然具有较强的肿瘤抑制功能,而定位于细胞核内的PTEN蛋白主要行使磷酸酶非依赖的功能,提示核PTEN蛋白在肿瘤抑制功能中的重要性。但是,目前关于核PTEN的抗肿瘤作用的分子机制尚知之甚少。陈国强课题组利用蛋白质相互作用组学技术,鉴定到136个与核PTEN相互作用的蛋白质。其中,38个属于剪接体的组成成分。进一步的研究发现, PTEN与剪接体蛋白紧密结合并且调控剪接体组装。在此基础上,他们利用蛋白质芯片技术,发现并证实PTEN能够和剪接体蛋白U2AF2直接相互作用,影响其被剪接体招募的过程。
真核生物的基因表达在RNA水平受到多个层面的精细调控。其中之一就是mRNA剪接,即移除前体mRNA中的内含子并拼接外显子成为成熟mRNA。可变或选择性剪接过程在不同组织和发育过程中都受到严密调控,其失调与包括肿瘤在内的许多疾病都密切相关。课题组借助高通量测序方法和生物信息学手段,发现核PTEN可以从整体层面调控前体mRNA的可变剪接,并鉴定了一批受到PTEN调控的可变剪接事件。通过分析肿瘤样本中这些可变剪接事件的发生频率、与PTEN的相关性以及与病人生存期的关系,发现相当一部分PTEN调控的可变剪接事件与肿瘤的发生发展密切相关。
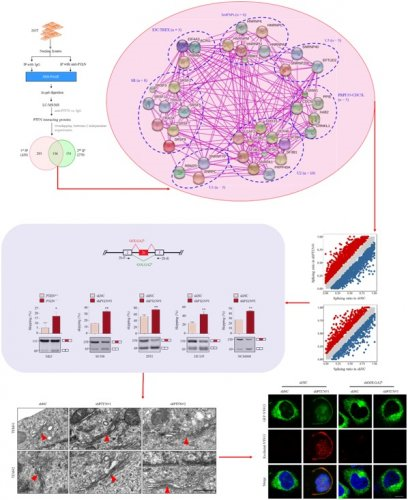
课题组发现,高尔基体相关功能基因GOLGA2的可变剪接是核PTEN所调控的可变剪接事件之一。PTEN缺失使得其在新定义的外显子2b处发生剪接跳跃,产生了更多不含有外显子2b的变体。这一可变剪接事件的发生使得高尔基体变得更为伸展,分泌功能大幅增强,进而介导了PTEN缺失肿瘤的生长优势。在此基础上,利用PTEN缺失细胞依赖于较强分泌功能的这一特点,课题组发现分泌抑制剂BFA和GCA能够选择性地杀死PTEN缺失的肿瘤细胞。这项研究不仅揭示了细胞核内PTEN蛋白发挥抑癌作用的全新机制,同时也为PTEN缺失肿瘤的靶向治疗提供了新的思路。
该论文由细胞分化和凋亡教育部重点实验室沈少明博士(同时为共同通讯作者)和上海生命科学研究院健康科学研究所冀颜博士为论文第一作者,陈国强教授为通讯作者。相关工作得到国家自然科学基金重点项目和创新研究群体、科技部重大研究计划等的支持。